CKD与免疫系统及炎症的关系:CKD影响免疫系统稳态,炎症是CKD常见特征。其炎症来源多样,内源性有细胞因子清除减少、肠道菌群失调等,外源性涉及感染、透析相关因素等。炎症在CKD各阶段逐渐加重,且因疾病病因不同存在差异。
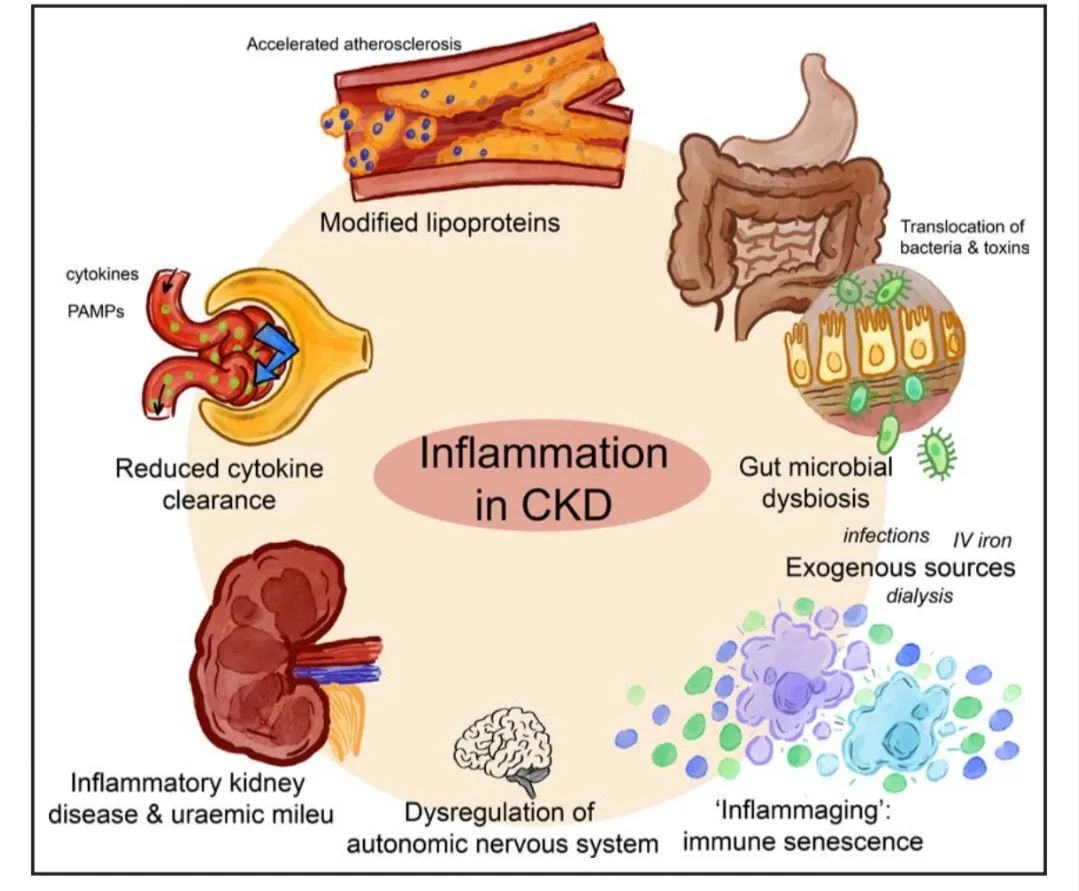
图1 慢性肾脏病(CKD)中的炎症来源。
PAMPs:病原体相关分子模式。
-慢性肾脏病(CKD)中的炎症来源多样。修饰脂蛋白会通过改变其蛋白质组和脂质组,促进炎症反应。循环细胞因子清除减少,使得促炎细胞因子如白细胞介素 - 1(IL-1)、白细胞介素 - 6(IL-6)等在体内积累,加剧炎症。肠道微生物群失调,肠道屏障功能受损,细菌毒素易位进入循环系统,激活免疫系统引发炎症。感染,包括导管相关血流感染、透析通路部位感染等,以及静脉注射铁剂(IV iron)治疗贫血时引发的氧化应激和炎症反应,均会加重炎症负担。透析过程中,透析用水杂质、透析液微生物质量以及透析回路中生物不相容的膜和溶液等因素,也会导致炎症激活。炎症性肾病会直接引发炎症,而尿毒症环境则通过多种机制,如代谢紊乱、毒素积累等,促进炎症发生。自主神经系统失调,交感神经过度活跃和副交感神经功能障碍,会干扰身体的正常调节机制,导致炎症加剧。免疫衰老使免疫系统功能下降,易引发炎症反应。“炎症衰老”是指在慢性肾脏病患者中,血管老化加速,炎症标志物水平升高,进一步加重炎症状态,影响心血管健康。病原体相关分子模式(PAMPs)可激活免疫系统,启动炎症反应。这些炎症来源相互作用,形成复杂的炎症网络,对慢性肾脏病的进展和患者的健康产生负面影响。
- Modified lipoproteins:修饰脂蛋白
- Reduced cytokine clearance:细胞因子清除减少
- Gut microbial dysbiosis:肠道微生物群失调
- Infections:感染
- IV iron:静脉注射铁剂
- Dialysis:透析
- Inflammatory kidney disease & uraemic milieu:炎症性肾病和尿毒症环境
- Dysregulation of autonomic nervous system:自主神经系统失调
- Immune senescence:免疫衰老
- 'Inflammaging':炎症衰老
- PAMPs:病原体相关分子模式(Pathogen-Associated Molecular Patterns的缩写 )
- Inflammation in CKD:慢性肾脏病中的炎症
炎症在CKD患者中风发病机制中的作用:多项研究表明炎症在CKD患者中风发生发展中起重要作用。实验模型显示CKD激活巨噬细胞促炎分子加速动脉粥样硬化;队列研究发现CKD患者炎症生物标志物升高,与心血管事件相关;遗传关联研究证实相关基因变异与炎症、中风风险有关;临床试验表明抗炎干预对降低心血管事件风险有潜在益处。
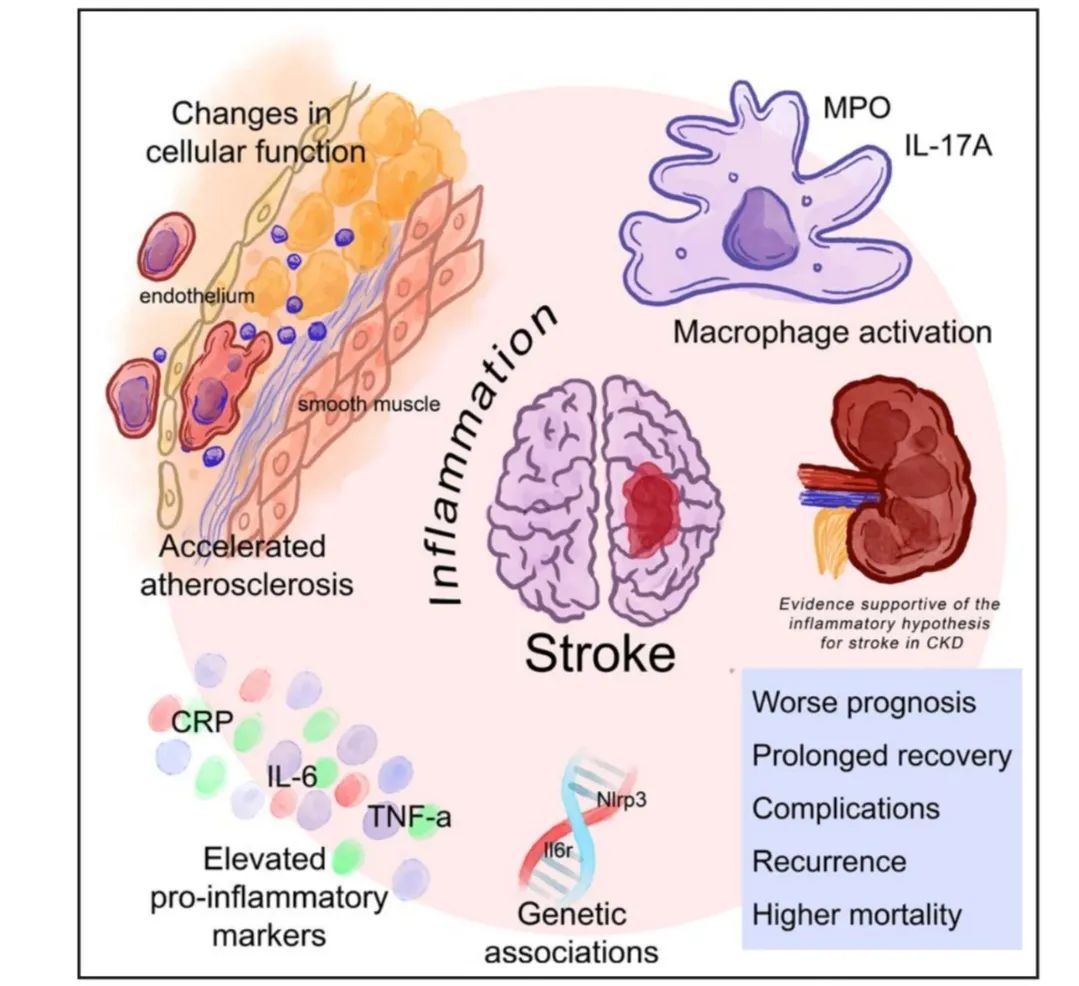
图2支持慢性肾脏病(CKD)患者中风炎症假说的证据:在慢性肾脏病(CKD)患者中,炎症在中风的发生和发展过程中起着重要作用,有诸多证据支持这一炎症假说。从细胞层面来看,炎症会导致细胞功能发生改变,巨噬细胞被激活,释放髓过氧化物酶(MPO)和白细胞介素17A(IL-17A)等物质。这些物质会增加斑块负担,加速动脉粥样硬化进程,使血管壁逐渐增厚、变硬,血管狭窄,增加中风的风险。炎症还会影响内皮细胞的正常功能,破坏血管内皮的完整性,导致内皮功能障碍,进一步影响血管的正常生理功能。炎症会导致C反应蛋白(CRP)、白细胞介素6(IL-6)、肿瘤坏死因子α(TNF-α)、NLRP3等炎症标志物水平升高。这些升高的炎症标志物与中风的不良预后密切相关,会导致中风病情更严重,患者的神经功能缺损更明显,恢复时间延长,同时还会增加并发症的发生风险,如感染、深静脉血栓形成等,并且会使中风的复发风险显著增加,患者的死亡率也随之上升。从遗传关联方面来看,特定的基因变异与炎症水平以及中风风险之间存在紧密联系。例如,某些基因变异会影响炎症相关信号通路的正常功能,导致炎症反应失调,进而影响中风的发生和发展。这些证据共同表明,炎症在慢性肾脏病患者中风的发病机制中起着关键作用,为进一步研究和治疗提供了重要依据。
Inflammation(炎症)、Stroke(中风)、CRP(C反应蛋白,全称C-Reactive Protein )、IL-6(白细胞介素-6,全称Interleukin-6 )、TNF-a(肿瘤坏死因子-α,全称Tumor Necrosis Factor-alpha )、MPO(髓过氧化物酶,全称Myeloperoxidase )、IL-17A(白细胞介素-17A,全称Interleukin-17A )、Nirp3(可能是NLRP3的误写,NLRP3即NLR家族含pyrin结构域蛋白3,全称NLR Family Pyrin Domain Containing 3 )、atherosclerosis(动脉粥样硬化)、cellular function(细胞功能)、endothelium(内皮)、Macrophage activation(巨噬细胞激活)、smooth muscle(平滑肌)、Worse prognosis(更差的预后)、Prolonged recovery(恢复时间延长)、Complications(并发症)、Elevated(升高的)、Recurrence(复发)、Genetic associations(遗传关联)、Higher mortality(更高的死亡率) 。
炎症对中风预后的影响:CKD相关炎症影响中风各个预后指标。它会加重中风严重程度,导致更大梗死体积和更严重神经功能缺损;阻碍中风后恢复,影响神经可塑性;增加非血管性并发症风险;加速动脉粥样硬化和内皮功能障碍,使患者易发生复发性中风和其他血管事件;还与CKD患者较高死亡率相关。
抗炎治疗策略:目前有多种针对CKD患者中风的潜在抗炎治疗方法。抑制IL-1β、IL-6的药物在部分试验中显示出降低炎症指标、改善心血管功能的效果;传统药物如秋水仙碱虽有广泛抗炎作用,但在CKD患者中使用存在安全性问题;他汀类、SGLT2抑制剂等具有多效性,在降低中风风险方面有一定作用;GLP-1受体激动剂和非甾体盐皮质激素受体拮抗剂也展现出抗炎及保护心血管的效果。
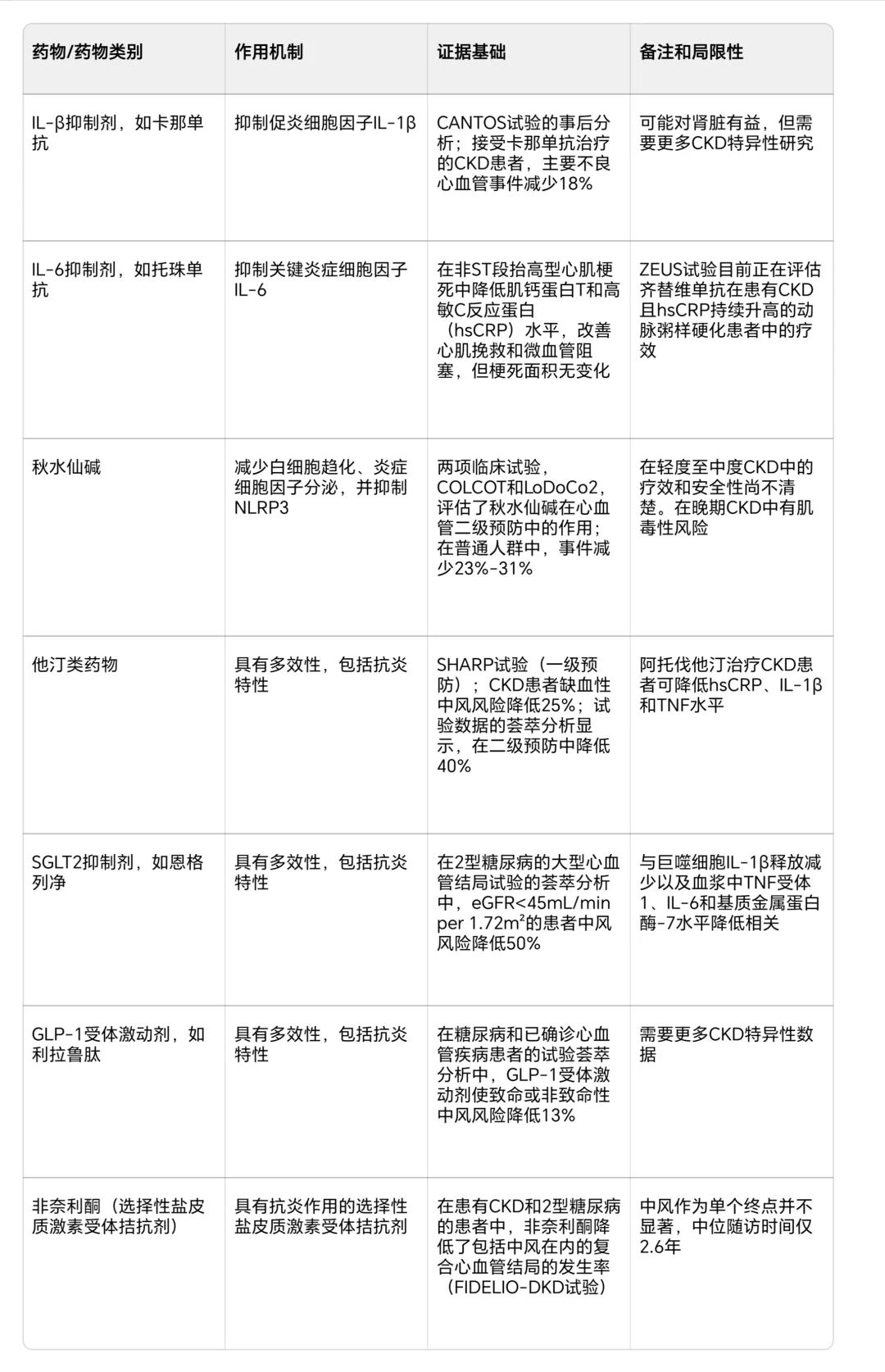
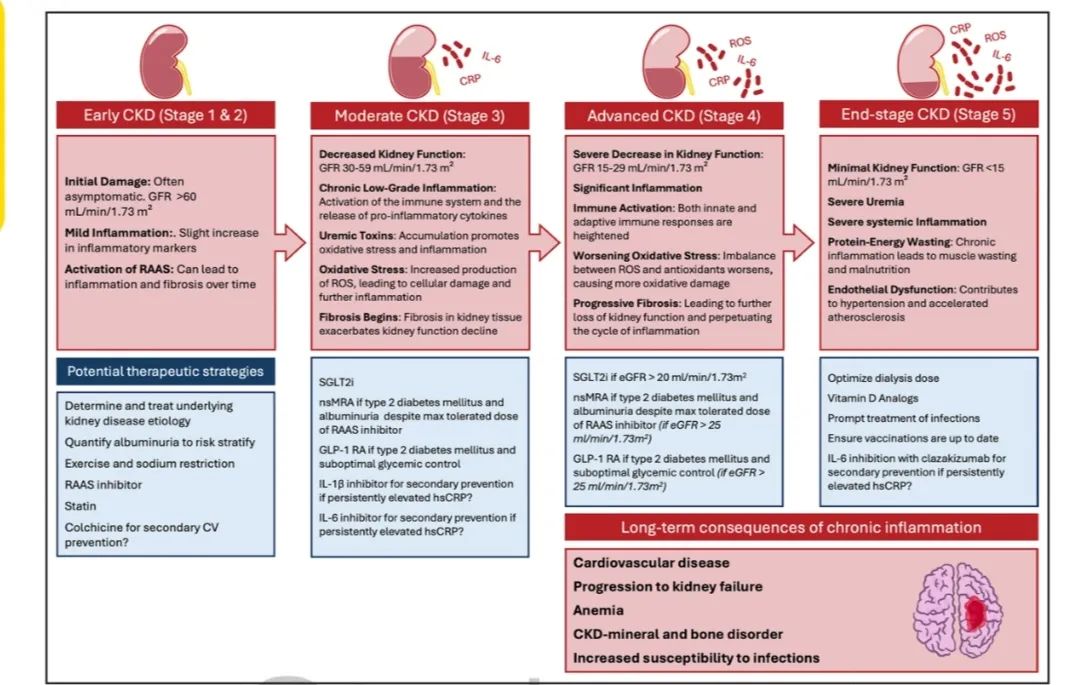
图3 基于慢性肾脏病(CKD)分期和进展的拟议炎症靶点和治疗策略
- 早期CKD(1期和2期):此阶段常出现初始损伤,炎症处于轻度状态,表现为炎症标志物略有升高。治疗策略包括确定并治疗潜在的肾脏疾病病因;量化白蛋白尿以进行风险分层;使用肾素 - 血管紧张素 - 醛固酮系统(RAAS)抑制剂;若估算的肾小球滤过率(eGFR)>20ml/min/1.73m²,可使用钠 - 葡萄糖协同转运蛋白2抑制剂(SGLT2i);控制血糖不佳的2型糖尿病患者,可使用胰高血糖素样肽 - 1受体激动剂(GLP-1 RA);及时治疗感染并确保疫苗接种最新;进行运动和限制钠盐摄入。
- 中度CKD(3期):该阶段炎症较为明显,尿毒症毒素积累,促进氧化应激和炎症,炎症过程开始导致肾脏组织纤维化,加重肾功能下降。治疗策略主要是继续优化早期的治疗措施,对于2型糖尿病患者,可考虑使用非甾体盐皮质激素受体拮抗剂(nsMRA)。
- 晚期CKD(4期):此时免疫激活增强,先天和适应性免疫反应都有所提高,氧化应激恶化,肾脏纤维化进展。治疗上除延续之前的策略外,对于持续高敏C反应蛋白(hsCRP)升高的患者,可考虑使用IL - 1抑制剂进行二级预防。
- 终末期CKD(5期):会出现严重尿毒症和全身性炎症,炎症标志物达到峰值。治疗方面,需优化透析剂量;若存在维生素D缺乏,可使用维生素D类似物。
未来研究方向:未来应开展针对CKD患者的大规模临床试验,评估抗炎药物安全性和有效性;探索联合治疗方案;研究长期效果;确定预测中风风险和治疗获益的生物标志物;深入研究炎症致病机制;评估药物安全性;收集真实世界证据;开展药物基因组学研究;关注患者中心结局和成本效益分析。
结论:CKD、炎症和中风之间关系复杂。控制炎症及病因可能是降低CKD患者中风风险的策略,但还需考虑年龄和多种合并症等因素。未来需更多研究明确抗炎治疗在该患者群体中的作用 。
参考文献
Kelly, D. M., Kelleher, E. M., & Rothwell, P. M. (2025). The Kidney-Immune-Brain Axis: The Role of Inflammation in the Pathogenesis and Treatment of Stroke in Chronic Kidney Disease. Stroke, 56(00), 00 - 00. DOI: 10.1161/STROKEAHA.124.047070
联系人:吴晨雪
手机:15602945134
电话:0755-32960208
邮箱:rosellebio@126.com
地址: 广东省深圳市盐田区壹海中心1203室